09级校友朱云麓“出人意料的发现”不意外的刊登Cell
9月5日,朱云麓(0908)以第一作者身份在《CELL》杂志发表了题为“Migratory Neural Crest Cells Phagocytose Dead Cells in the Developing Nervous System”的研究。该研究发现了神经嵴细胞的隐藏功能。
以下研究内容来源于朱云麓(0908)在BioArt微信公众号撰写的《一作解读Cell | 出人意料的发现,早期神经系统发育过程中的清道夫》(以下简称《解读》)
细胞是生物体结构和功能的基本单位,而在你我体内,每时每刻却有成千上万的细胞死去,或是由于细胞病变,或是为了控制细胞数目,维持组织更替。比如,人体内小肠上皮细胞每 2-3 天就会更新一次,以维持正常的肠道功能。这些死去细胞的碎片通常会被来自免疫系统的吞噬细胞(phagocytes)迅速清除,以确保机体微环境的稳定,避免发生炎症反应。细胞死亡不仅仅发生在成熟的个体中。脊椎动物胚胎在生长发育产生大量新细胞的过程中,为了调整形态发生、控制组织大小、剔除不健康的细胞,也有数不清的细胞被判死刑。最为夸张的是在神经系统发生时,早期神经干细胞分化分裂出 2 倍之余所需的神经细胞和胶质细胞,在之后的细胞分化和神经网络搭建过程中,多余的细胞全部会死去,产生大量的细胞碎片。然而,在早期胚胎发育阶段,负责清除死细胞的免疫系统还没完全成熟,与此同时,神经系统早已迫不及待地开始搭建。那么,究竟是什么机制确保了早期胚胎中的死细胞能被迅速清除呢?发育生物学家们被这个问题困扰多年。
2019 年 9 月 5 日,弗吉尼亚大学Sarah Kucenas实验室在Cell杂志发表了题为Migratory Neural Crest Cells Phagocytose Dead Cells in the Developing Nervous System的研究。这项工作揭示了一类发现于 100 多年前、被大量研究的细胞——神经嵴细胞——出人意料地在神经系统发育的早期高效吞噬死去的细胞。之所以称之为“出人意料”的发现,不仅是因为神经嵴细胞在之前早已被研究得非常多但它们的这项功能却并未被报道,也由于这个发现本身来自一点点的意外以及我们对科研结果的好奇心。希望能通过下面的内容,向大家展示我们的研究成果以及它背后的故事。
图片来源于《解读》
1试验方法
我们使用了模式动物斑马鱼,并充分利用斑马鱼胚胎透光性的特点,结合了活体激光共聚焦显微镜术,来研究这个问题。
为什么要使用斑马鱼而不是更为常见的小鼠来作为模式生物呢?由于清除死细胞的吞噬过程发生得非常迅速,并且我们感兴趣的阶段是在胚胎发育早期,在小鼠、大鼠等体内发育的模式生物中无法进行高时间分辨率的成像。而斑马鱼同为脊椎动物并且在体外受精发育,利用其胚胎良好的透光性,可以进行高空间、时间分辨率的活体显微延时摄影。
但是,细胞又不会自己发光。如何才能使用荧光标记我们感兴趣的细胞呢?这里我们就利用了斑马鱼另一个特性:能够快速、便捷、稳定地在特异细胞中表达指定荧光蛋白。
我们知道,不同种类的细胞会有选择地表达一些不同的基因,而调控基因表达的启动子和增强子通常位于基因片段的上游。利用这点,我们可以人工搭建质粒,将特异表达在目标细胞中的某基因上游的 DNA 片段与指定的荧光蛋白连接,并将质粒插入到斑马鱼胚胎的基因组中。那么,目标细胞在表达这个基因的同时,也会启动我们插入片段中荧光蛋白基因的表达。如此一来,目标细胞就会被荧光蛋白所特异标记。再利用活体显微光学成像,我们就可以在斑马鱼中观察到表达荧光蛋白的细胞了。随着近年来各种各样的荧光蛋白被开发出来,我们可以根据需要表达不同颜色、不同性质的荧光蛋白,有的能特异标记细胞核或细胞膜,而有些又能紫外照射下改变激发光的颜色。利用这项工具,我们可以灵活地搭建各种质粒,从而创造出研标记各类细胞的转基因斑马鱼。
2研究背景
什么是神经嵴细胞?它们在神经系统发育过程中又承担着什么功能?在神经系统发生的最早期,神经板中周围的外胚层向上方隆起,并在顶端闭合,形成神经管。神经管的内部会在之后发育成为脑和脊髓,也就是中枢神经系统。在神经管闭合过程中(或闭合后)位于其顶端神经嵴的细胞摆脱其原先的上皮细胞形态,转化成为具有强迁移力的间充质状细胞。这些向外脱离开的多能神经嵴细胞在经管外壁外侧沿着特定的通路向下方迁移,最终分化成为色素细胞、颅面部细胞、骨细胞、平滑肌细胞,以及外周神经元和胶质细胞。由此可见,神经嵴细胞是一种重要的、进化保守的、具有高迁移力的细胞。那么,我们是如何发现并证明神经嵴细胞具有吞噬功能的呢?
3研究结论
3.1. 新的外周和中枢神经系统死细胞清除机制
为了探究躯干神经嵴细胞是否能在发源于卵黄囊的免疫系统早期吞噬细胞到来之前吞噬死细胞,我们使用转盘激光共聚焦显微技术(spinning disk confocal microscopy)在活体斑马鱼胚胎中拍摄荧光标记的神经嵴细胞,并将 20 多个小时的拍摄图像制成显微缩时电影。我们发现,在发育中的胚胎内有死细胞出现时,一些神经嵴细胞会脱离原有的迁移路线,转而向着细胞碎片迁移过去,有的细胞甚至会爬行将近 100 微米的距离。当接近细胞碎片时,它们会张开“大口” (吞噬杯) ,将死细胞吞入胞体内,形成球形的吞噬体。这些吞噬体会与早期内体、晚期内体和溶酶体依次结合,从而不断酸化体内空间,以降解吞噬后的细胞碎片。这些神经嵴细胞好像并无忌口,会吞噬各种各样的死细胞,包括其他神经嵴细胞、神经元和肌肉细胞。有时,肌肉细胞个头太大,无法被一个神经嵴细胞吞噬,则多个细胞会被吸引过来,围绕着肌肉细胞旋转,试图分食细胞碎片。
视频:绿色荧光标记的神经嵴细胞形成吞噬体并逐渐酸化 (红色)
令人震惊的是,本应待在外周神经系统的神经嵴细胞,有时竟可以通过运动神经轴突中枢-外周神经系统过渡区(motor exit point transition zones),进入脊髓,清除脊髓下侧的死细胞!通常进入中枢神经系统的神经嵴细胞会在脊髓内待上几到十几小时不等,然后爬出脊髓,回到外周神经系统。
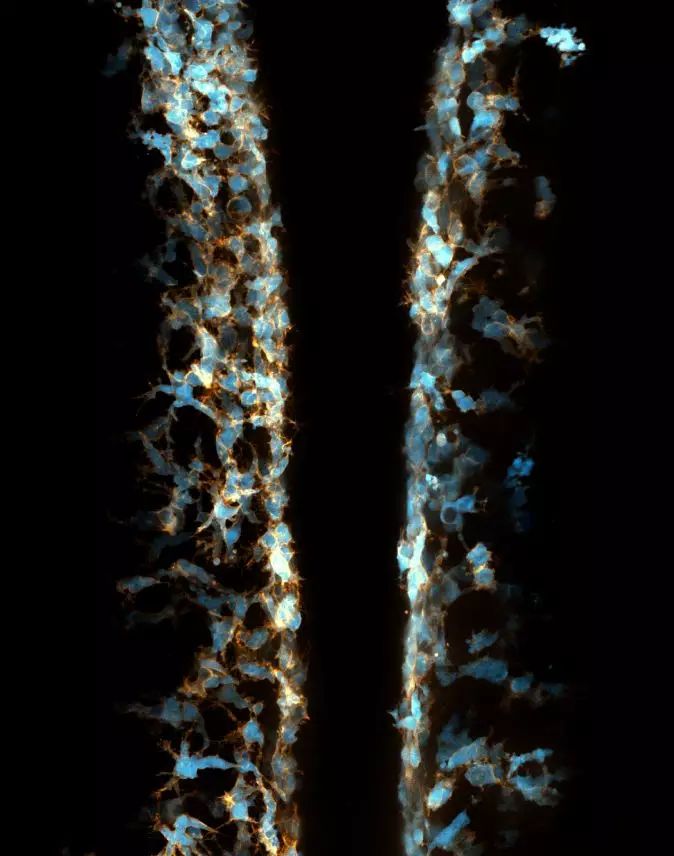
图:两个背靠背的、神经嵴细胞被荧光标记的斑马鱼胚胎的侧视图。神经嵴细胞的细胞膜与细胞质分别被标记为橙色与蓝色(来源于《解读》)
3.2. 吞噬能力不由细胞谱系决定但与发育时间相关
在我们拍摄的电影中,多数时候并不是死细胞并不是被距离最近的神经嵴细胞清除。是否存在一个特定族群的神经嵴细胞具有吞噬功能呢?
由于神经嵴细胞的多能性,我们首先探究这些吞噬性的细胞是否属于一个特定的神经嵴谱系。活体显微技术的另一个优点是使得我们能够在拍摄的同时对于目标细胞进行操控,为了标记单个细胞并对其进行追踪,我们在表达可变色荧光蛋白的斑马鱼中,使用氮脉冲激光(nitrogen pulsed laser)瞄准并发射紫外光照射单个具有吞噬功能的神经嵴细胞,将其荧光蛋白激发波长从绿色光转为红色光。令人意外的是,谱系追踪结果显示,会吞噬的神经嵴细胞最终分化成为了多种多样的细胞,说明它们并不属于某个特定的谱系。
由于在自然状态下,大约只有 5% 的神经嵴细胞进行了吞噬行为。那么,通过制造更多的死细胞,我们能够激活更多神经嵴细胞进行吞噬么?于是,我们使用了氮脉冲激光瞄准并杀死个别细胞,观察神经嵴细胞对细胞死亡的反应。令人惊奇的是,在诱发细胞急性死亡后极短的时间内,周围的神经嵴细胞纷纷向死细胞张开大口。这个结果说明诱导细胞死亡可以触发神经嵴细胞的吞噬行为,也支持多数神经嵴细胞都具有潜在吞噬能力的假说。
另外通过推迟诱导细胞死亡的时间并比较神经嵴细胞在不同时期的转录组,我们发现神经嵴细胞的这种吞噬能力随着生长发育的行进而慢慢退去。但究竟是由于它们开始分化成其他细胞而丧失了高效的吞噬能力,还是以巨噬细胞为主的吞噬细胞的到来抑制了神经嵴细胞的吞噬,目前还不得而知。
3.3. 白细胞介素-1β
过去的许多工作展示了神经嵴细胞保守、鲁棒的迁移通路,我们的研究却发现它们能被死细胞所吸引,离开固有的迁移通路,神经嵴细胞又是如何知晓死细胞的位置?
通过诱导细胞死亡,观察神经嵴细胞迁移的同时,我们将斑马鱼胚胎浸润在各种信号通路抑制剂中,寻找神经嵴细胞聚集被削弱的表形。我们发现,在半胱氨酸蛋白酶(Caspase)-1抑制剂与白细胞介素-1β抑制剂的作用下,神经嵴细胞向细胞碎片的聚集能力显著下降。有趣的是,免疫荧光与转基因斑马鱼活体成像结果显示,死细胞与神经嵴细胞都可以表达白细胞介素-1β!这个结果展示了白细胞介素-1β在维持生物稳态中的作用。另外,与其他严重损伤实验模型(列如细菌感染后)相比,我们检测到的白细胞介素-1β水平显著偏低。也同时,支持了之前研究提出的假设:在不同刺激下的白细胞介素-1β的释放量决定了它引起的免疫反应的激烈程度,因此会被严格控制。
4意料之外,情理之中
在 2014 年初,我被斑马鱼活体显微荧光技术的美妙所吸引,加入了 Kucenas 博士的研究组。我最初的课题是研究神经束膜胶质细胞(perineurial glia)在胚胎发育过程中与运动神经元和神经嵴细胞的相互作用。在拍摄细胞质被荧光标记的神经嵴细胞迁徙过程中,我意外地发现个别神经嵴细胞的移动轨迹有所异常,而且一些细胞中还有着 3-10 微米的圆形空洞。在查阅了各种研究论文之后,我发现神经嵴细胞的这类行为并未被描述过,这引起了我强烈的好奇心,我也因此将研究重心转移到神经嵴细胞。在去年(2018)年底,这项工作的大部分实验已经完成,但是由一个问题一直在我脑海中挥之不去,那就是究竟神经嵴细胞是如何知晓死细胞的存在的呢?为了寻求免疫学专业人士的帮助,我与多个专攻细胞吞噬和神经免疫的教授探讨了这个问题。在他们的建议下,我们尝试抑制了多种经典吞噬过程中的搜索识别通途,但都没获得很好的效果。碰巧我们另一个项目的合作实验室有半胱氨酸蛋白酶抑制剂,于是便拿来试了一下,谁知就打开了一扇新的大门。
神经嵴细胞的这个功能出乎我们所有人的意料,但仔细想想,却又在情理之中。在这项工作大体成型后,我将这个故事与研究神经嵴细胞十几年的老教授分享,并询问他们以前是否见过这种现象,他们纷纷表示,可能见到过,但却没有当回事儿。
以上是我想与各位分享的一些研究经历,希望在科研前线奋战的同学们能从中获得一些启发和动力。
其实这此我们发表的小故事还有着许多谜点,最有意思的一个问题就是,既然许多神经嵴细胞的吞噬功能都会被诱导的细胞死亡激活,为什么在生理状态下并不是距离最近的神经嵴细胞参与碎片清除呢?这个问题也留给各位读者思考。
最后,借用美国棒球运动员 Yogi 的一句话来作为结尾,我认为它准确地阐述了活体成像技术的美妙:“You can observe a lot by just watching.”
原文链接:https://www.cell.com/cell/pdf/S0092-8674(19)30889-X.pdf
朱云麓校友简介
朱云麓,0908,2009年考入中国科学技术大学生物系。于2013年获得中国科学技术大学生命科学学士学位,其后于2019年获得美国弗吉尼亚大学生物学博士学位。现于纽约大学医学院进行博士后研究,主要研究方向包括斑马鱼神经系统发育,前庭神经通路和神经退行性疾病。
2019-12-04 上一篇: 七中国科大人晋IEEE会士 下一篇: 三中国科大人晋ACM Fellow




 京公网安备 11010802035836号
京公网安备 11010802035836号